专访兆科眼科董事会主席李小羿:当下最要紧是拿到阿托品“入场券”
每经记者 陈星 每经编辑 杨夏
2021年4月29日,兆科眼科赶上了港股18A(香港交易所新《上市规则》的“主板上市规则”第十八A章)的末班车,成功挂牌上市。兆科眼科是一家资本市场上的新兵,但其创始人、董事会主席李小羿却是一名医药行业的老将。
早在1994年,李小羿就一手创办了李氏大药厂。2017年,李小羿将眼科管线从李氏大药厂中分拆出来,成立了兆科眼科,正式投身到眼科药物的开拓中去。眼下,兆科眼科用于治疗干眼症的环孢素A眼凝胶正在申报上市,用于延缓青少年近视进程的阿托品滴眼液正处于Ⅲ期临床——兆科眼科正处于收获期来临前夜。
李小羿说,眼科药物是一个长期被忽视的领域,“因为盘子小,资本也不关注”。但眼科药物需求却十分庞大,不仅数量巨大,对新药、好药的需求也尤为迫切。
根据世卫组织2020年发布的《世界视力报告》,全球至少有22亿人患有视力损伤或盲症。其中至少10亿人的视力损伤问题本可预防或尚待解决。
但与眼部疾病高发病率相对应的,是我国眼科制药的市场空间大约只占整个眼科赛道的10%,处于较低位置。核心原因还是研发难度大、临床试验导致等待周期长、药品获批上市后依然有较高淘汰率等。
李小羿说,包括眼药行业在内,整个生物医药行业正处于钟摆效应的过程中,在经历过热与过冷后逐步回归中间地带。这其实就是大浪淘沙之后回归理性,对于一些真正去做研发创新的企业,这是好事。
阿托品滴眼液进入加时赛
眼科药物领域一场最接近公开透明的比赛,应该是阿托品滴眼液的竞速赛。
这种M胆碱受体抑制剂药物早在2005年前后就在新加坡、中国香港等地开展用于延缓青少年近视发展的研究,但在中国内地,尚无正式获批的阿托品滴眼液。此前,一些企业利用政策“擦边球”在互联网医院销售阿托品院内制剂,但在今年被叫停网售。在这种背景下,率先成为青少年近视防控领域的“正规军”,成为众多企业梦寐以求之事。
聚焦到赛道上,竞争更加激烈。药物临床试验登记与信息公示平台显示,本土药企中,兴齐眼药、欧康维视、兆科眼科、恒瑞医药已经将阿托品滴眼液的临床试验推动到了Ⅲ期阶段。其中,兴齐眼药和兆科眼科的Ⅲ期临床试验显示受试者已经招募完成,试验正在进行中。
不出意外,头名也将在这两家企业中诞生。今年9月,兴齐眼药方面在与投资者交流时表示,2年期的Ⅲ期临床试验已经完成试验招募,处于随访阶段。
兆科眼科则属于“另辟蹊径”。2020年,兆科眼科与美国Nevakar签订协议,引入后者开发的低浓度硫酸阿托品在大中华区、韩国等地区开发和商业化权益。2021年9月,兆科眼科NVK002为期两年的Ⅲ期临床试验(针对近视加深的儿童阿托品研究,又称“中国 CHAMP”研究)及为期一年的第Ⅲ期桥接临床试验(小型CHAMP),获国家药监局批准。
今年8月,兆科眼科宣布两项试验均提前数月完成患者入组,使兆科眼科在阿托品滴眼液的研发中占据领先位置。
如今阿托品滴眼液的竞速赛进入加时阶段,但研发企业丝毫不敢放下悬着的心。在接受《每日经济新闻》记者专访时,李小羿坦言,“眼下最重要的,就是拿到阿托品滴眼液的入场券”。
《每日经济新闻》记者注意到,《中华人民共和国药品管理法实施条例(修订草案征求意见稿)》提出了“独占期”概念,即对首个批准上市的儿童专用新品种、剂型和规格,以及增加儿童适应症或用法用量的,将给予最长不超过12个月的市场独占期,期间内不再批准相同品种上市。
这意味着,谁能抢到第一名,谁就拥有最长不超过一年的市场独占期。这一诱惑显然是巨大的,但撞线并非易事。记者了解到,阿托品迟迟未在中国内地获批,有其特殊原因。
全国防盲技术指导组组长、首都医科大学附属北京同仁医院眼科中心主任王宁利,同时也是兆科眼科NVK002第Ⅲ期临床试验牵头研究者。王宁利在接受《每日经济新闻》记者采访时表示,在西方国家,近视并不是一个亟待解决的临床需求,因此未在该类药物上投注太多资源精力。但亚洲青少年近视高发,尤以我们国家的青少年近视率畸高且还在持续增长,所以我们需要在欧美药物成熟市场之前去批准阿托品滴眼液上市,“第一口吃螃蟹”注定要更慎重。
王宁利继续说明,儿童青少年用药是一个尤为严肃的问题,我国针对阿托品滴眼液的临床试验设计期限是3年,临床试验可以观察到3年内的安全性和有效性,但该药物是一个长期使用的药品,当大范围、长时期应用后,药品的安全性和有效性如何?这是需要观察的。
王宁利指出:“阿托品滴眼液要获批,我们不仅需要药物注册试验的数据和结果,也需要上市后更长的观察期。”
可以看到,无论是药监机构,还是业内顶尖专家,对阿托品都持谨慎观察态度。阿托品滴眼液想要拿到批文,还要继续等待。对于研发企业而言,上市“分秒必争”。李小羿在采访中感叹,“只要阿托品滴眼液上市,无论上市后需要多长的观察期都愿意”。
对于兆科眼科来说,还有另一个选择。即阿托品的海外合作伙伴正在海外进行Ⅲ期临床,一旦在海外率先获批,再反向引进到国内申请注册,也不失为一种方法。“这条路说不定会更快。”王宁利说。
眼科赛道不惧“内卷”?
比起在阿托品身上的急迫,在干眼症药物环孢素A眼凝胶上,兆科眼科可以暂时松一口气。
今年6月,兆科眼科宣布环孢素A眼凝胶的新药申请获国家药监局药品审评中心受理。环孢素A眼凝胶进入上市倒计时阶段,该药物还将成为兆科眼科首款商业化的自主开发创新药。
干眼症的用药需求不逊于近视防控。弗若斯特沙利文报告显示,预计国内中重度干眼病药物市场将由2024年的3亿美元增加至2030年的16亿美元,复合增长率为34.1%。作为干眼症的“明星”药物,艾尔建公司的Restasis年销售额曾突破10亿美元。
国内,也已有Restasis的首仿药上市并纳入医保。
李小羿认为,对比市面上的环孢素产品,兆科眼科的环孢素A眼凝胶具有差异化优势。其凝胶剂型起效更快,且具有每天只需给药一次的优点,依从性更佳。
更多竞争者也瞄准了干眼症市场。今年3月29日,恒瑞医药宣布SHR8028滴眼液新增一项Ⅲ期临床试验申请获得NMPA(国家药品监督管理局)批准。SHR8028是一款恒瑞医药于2019年引入的干眼症药物。与此同时,更多仿制药也被推向市场。
这带来了一个隐忧,眼前节疾病包括三大适应症——近视、干眼症和老花眼,竞争已如火如荼,眼药研发企业如何避免陷入“内卷”困境?
对此,李小羿对记者表示,中国的眼科药物供应和需求之间还存在巨大的错配。他说:“以干眼症药物为例,国内有药物上市之前,干眼症患者只能使用人工泪液缓解。从市场数据来看,人工泪液的市场规模一度非常庞大,当环孢素药物上市之后迅速进入医保,都说明了干眼症还有巨大的未满足的临床需求。因此不管是几个药物,市场需求摆在那里,不仅有规模还有紧迫性。”
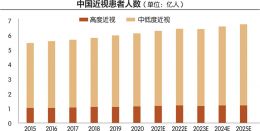
王宁利也认为,虽然阿托品滴眼液已经有五六个药物在排队,“扎堆”现象肯定存在,但同时也要看到近视等疾病已经上升为公共卫生问题,中国总人群的近视患病率超过50%,约7亿人口的规模。因此市场是巨大的,眼科企业应该不惧怕“内卷”。
市场虽然广阔,但同其他新药研发的思路一样,眼药也要做出差异化。王宁利就提到,以阿托品滴眼液为例,其一早期研究论文早已发表,其二不同浓度并不能作为专利。因此,只能从减轻副作用、舒适度、剂型和生产工艺等方面做出差异化。据了解,兆科眼科的阿托品滴眼液可解决低浓度阿托品的不稳定性,且不含防腐剂,预计保存期超过24个月,在副作用、便利性等层面有创新改良。
而在现有药物方面,我国的眼药研发企业也大有可为。
另一眼科药物代表企业就曾在接受《每日经济新闻》记者采访时表示,眼底药物通常所需的眼底注射方式无论对于患者还是医疗机构来说,都是较大的医疗负担,对于患者的依从性、安全性等都带来了考验。
李小羿也提到了这一点,之所以眼底药物在国内的整体渗透率很低,是因为现有药物带来的巨大治疗负担。怎么去解决这个问题,怎么创新和突破,是国内的眼药企业需要去做深的。
据李小羿介绍,近年来眼科领域很多重要突破集中在基因治疗上,他相信这种创新疗法还将在未来十年大展身手。“一方面,许多遗传性的眼科疾病与感光细胞有关,基因疗法能够将健康的基因引入到眼底,从而直接对疾病进行治疗。另一方面,眼睛周围环境相对封闭,不大会对外来物质产生免疫反应,这种‘免疫豁免’尤其利于基因治疗。”
今年,王宁利还曾公开提到:“现行的《国家基本药物目录(2018年版)》中的许多药品已经不能适应当前眼部疾病状况和满足临床诊疗需求,建议调整目录,纳入更多更适应中国眼科疾病变化需求、疗效更好、临床价值更高的眼科用药并适当调出目录内已经停产及临床使用较少、副作用较大的眼科老药。”
总体言之,国内眼药的需求庞大,对新药、好药的需求更加旺盛,国内研发企业如何跟进满足当前临床需求,是眼药企业的机遇之所在。
现在才是眼科药物黄金时期
2017年,年近六旬的李小羿将眼科管线从李氏大药厂中分拆出来,成立了专门从事眼科药物开发的子公司——兆科眼科。真正投身眼科药物研发五年,李小羿说,现在才是眼科药物的“黄金时期”。
“过去眼科药物不太受重视,传统药企认为这个领域太小,过去近视靠激光手术就解决了,没有人想到要用药防控。盘子小的时候,资本也觉得没有吸引力。”李小羿表示。
长期的忽视或者说重视不足,让国内的眼药研发还有相当长一段路要走。眼下,国内眼科用药仍以跨国企业主导,专注眼科的创新药企数量仍少;以基因治疗为代表的创新疗法在眼科领域研发火热,中国眼科创新疗法布局仍少,研发前景也面临多重挑战。
根据动脉网《2022眼科行业研究报告》,国内重点省、市公立医院眼科用药中,进口药物占比超过了50%。眼科用药市场的前4名分别是占比25.35%的瑞士诺华、占比14.24%的日本参天、占比6.32%的德国URSAPHARM、占比4.71%的我国企业兴齐眼药。
追赶离不开持续不断的动力,动力除了来自外部资本,更重要的得靠自己。今年以来,多家新药企业“一边研发、一边受伤”,面对退潮的资本和捉襟见肘的经济实力,有人选择停掉还遥遥无期的在研项目,有人收紧开支裹紧棉衣过冬。
在医药行业和资本市场都摸爬滚打多年的李小羿坦言已经见惯了这种潮起潮退。李小羿坦言,上市企业的优势是可以被资本看到,但资本的支持不会没完没了。且不同市场的资本视角是不同的,如美国资本市场会看到一个好的临床数据或完成不同临床试验的节点,给予奖励。但国内来说,更重要的是看到成果,看这个产品卖得怎么样。
“对一个企业来说,最重要的任务首先是生存,是尽快有现金流。所以我们一定要有产品可以尽快让大家看到,这样才能给自己争取时间。而做纯粹的新药需要更多时间、更多耐心,更多的是企业要保证自己经得起一些失败。”
兆科眼科的财务数据显示,自去年4月上市后,凭借IPO募集资金,目前公司拥有超过20亿元现金储备支持未来2~3年的产品研发。今年上半年,公司研发支出为1.01亿元。公司预计,除多个项目进入Ⅲ期临床需要增加研发投入外,2022年还将增加销售和营销支出,来支持产品商业化的落地。
李小羿表示,兆科眼科希望尽快通过自己的商业化实现自身造血循环,让公司可以自己运转下去。
“很多事情都是钟摆效应,最后停留在中间位置。这其实就是大浪淘沙之后回归理性,对于一些真正去做研发创新的企业,这是好事。估值疯狂的时候,一家公司融到很多钱的压力也很大,原本应该做得更扎实的东西会去求速度,并不是好事。”
李小羿最后说:“钟摆反复的过程中,大家应该更清楚地认识到医药行业的特性,这样行业才能健康发展。如果外界对我们抱有不现实的期望,那么很快就会失望,行业也会失去支持,这实际上是一个恶性循环。”